Carbono: propriedades e usos do elemento
Descrição
O carbono é um elemento não metálico que desempenha um papel fundamental nos processos vitais, nas aplicações industriais e na química. Ele tem propriedades químicas e físicas distintas que o tornam altamente versátil.

Introdução ao elemento
O carbono, simbolizado como "C" na tabela periódica, é um elemento químico com número atômico 6. É um dos elementos mais abundantes da Terra, encontrado tanto em organismos vivos quanto na crosta terrestre. Sua capacidade de formar ligações estáveis com muitos elementos, inclusive com ele mesmo, torna-o essencial para a vida como a conhecemos.
O carbono ocorre naturalmente em várias formas, principalmente como grafite, diamante e carbono amorfo (como o carvão). Ele também é um componente essencial das moléculas orgânicas, que são os blocos de construção da vida. As notáveis capacidades de ligação do carbono permitem a criação de uma vasta gama de compostos, tornando-o fundamental para a química orgânica.
Descrição das propriedades químicas
O carbono apresenta uma ampla gama de propriedades químicas. Uma das principais características é sua capacidade de formar ligações covalentes com vários outros elementos, inclusive hidrogênio, oxigênio, nitrogênio e ele próprio. Isso o torna altamente versátil na formação de diferentes tipos de moléculas. Aqui estão algumas das principais propriedades químicas do carbono:
- Comportamento de ligação: O carbono pode formar ligações simples, duplas ou triplas, dependendo do tipo de ligação que compartilha com outros elementos.
- Reatividade: Embora o carbono não seja altamente reativo em sua forma elementar (como grafite ou diamante), ele reage com o oxigênio em altas temperaturas para formar dióxido de carbono (CO₂). Ele também pode reagir com halogênios, hidrogênio e metais.
- Estados de oxidação: O carbono pode apresentar estados de oxidação de -4 (como no metano, CH₄), 0 (como no grafite ou diamante), +2 (como no monóxido de carbono, CO) e +4 (como no dióxido de carbono, CO₂).
- Alótropos: O carbono existe em vários alótropos, como diamante, grafite, grafeno e fulerenos, cada um com propriedades químicas diferentes devido ao arranjo dos átomos de carbono.
Tabela de dados de propriedades físicas
|
Propriedade |
Valor |
|
Número atômico |
6 |
|
Densidade |
2,267 g/cm³ (diamante), 1,550 g/cm³ (grafite) |
|
Ponto de fusão |
Sublima em torno de 3915°C (diamante) |
|
Ponto de ebulição |
Sublimação em torno de 3915°C (diamante) |
|
Dureza |
Muito dura (diamante), macia (grafite) |
|
Condutividade elétrica |
Conduz eletricidade (grafite, grafeno) |
|
Condutividade térmica |
Bom condutor (diamante) |
|
Cor |
Incolor (diamante), cinza/preto (grafite) |
Para obter mais informações, consulte Stanford Advanced Materials (SAM).
Usos comuns
O carbono é usado em uma grande variedade de setores devido às suas diversas propriedades físicas e químicas:
- Produção de aço: O carbono é um componente essencial na fabricação de aço, onde é usado para modificar as propriedades do ferro, tornando-o mais forte e durável.
- Negro de fumo: Usado como pigmento preto em tintas, pinturas e revestimentos.
- Eletrônicos: O grafite é usado em componentes eletrônicos como baterias, capacitores e como material de eletrodo.
- Filtragem: O carvão ativado é usado em sistemas de filtragem de água e ar para remover impurezas.
- Lubrificantes: As propriedades lubrificantes do grafite o tornam útil para reduzir o atrito em sistemas mecânicos.
- Diamante: Usado em ferramentas de corte e joias, o diamante é o material mais duro conhecido.

Métodos de preparação
O carbono pode ser obtido por vários métodos, dependendo da forma desejada:
- Do carvão: O carbono é extraído do carvão por meio de um processo chamado "carbonização", que envolve o aquecimento do carvão a altas temperaturas na ausência de oxigênio para produzir coque, uma forma pura de carbono.
- Grafite: O grafite de ocorrência natural é extraído, e o grafite artificial pode ser produzido por meio do tratamento de alta temperatura de materiais que contêm carbono, como o coque de petróleo.
- Diamante: Embora os diamantes ocorram naturalmente, os diamantes sintéticos podem ser fabricados usando métodos de alta pressão e alta temperatura ou deposição de vapor químico (CVD).
- Carvão ativado: Produzido pelo aquecimento de materiais ricos em carbono, como madeira ou cascas de coco, na presença de gases para criar um material poroso com alta área de superfície.
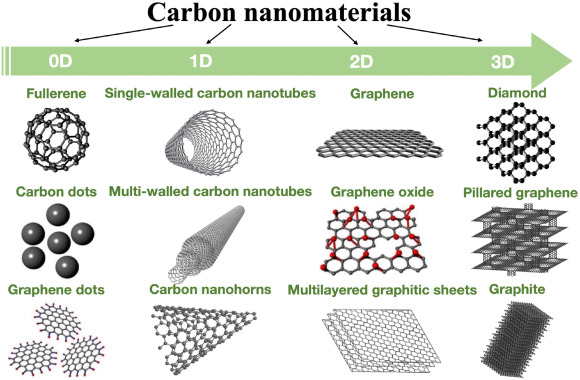 [1]
[1]
Produtos industriais relacionados
O carbono é fundamental para muitos processos e produtos industriais:
- Compostos de carbono: Usados nos setores aeroespacial, automotivo e esportivo para materiais leves e resistentes.
- Nanotubos de carbono: São usados em eletrônicos, dispositivos de armazenamento de energia e aplicações de nanotecnologia devido à sua resistência e condutividade.
- Dióxido de carbono (CO₂): Amplamente utilizado na produção de refrigerantes, extintores de incêndio e como refrigerante.
Perguntas frequentes
Qual é a forma mais comum do carbono?
O carbono é mais comumente encontrado na forma de grafite, diamante e carbono amorfo (como o carvão).
O carbono é tóxico?
O carbono em si não é tóxico em sua forma elementar, mas o monóxido de carbono (CO), um gás produzido pela combustão incompleta de combustíveis que contêm carbono, pode ser altamente tóxico.
Por que o carbono é importante para a vida?
O carbono é a espinha dorsal de todas as moléculas orgânicas, incluindo proteínas, lipídios e ácidos nucleicos, o que o torna essencial para os processos vitais.
Quais são os usos do carvão ativado?
O carvão ativado é usado em sistemas de filtragem, como purificadores de água e ar, para remover impurezas e toxinas.
Qual é a diferença entre o diamante e o grafite?
Embora ambos sejam feitos inteiramente de átomos de carbono, o diamante tem uma estrutura cristalina que o torna o material mais duro da Terra, enquanto o grafite tem camadas de átomos de carbono dispostas em uma estrutura planar que lhe permite ser macio e escorregadio.
Referências:
[1] Kuan Cheng, Samuel Wallaert, Haleh Ardebili, Alamgir Karim, Advanced triboelectric nanogenerators based on low-dimension carbon materials: A review,
Carbon, Volume 194, 2022, Páginas 81-103, ISSN 0008-6223, https://www.sciencedirect.com/science/article/pii/S0008622322002093

 Barras
Barras
 Miçangas e esferas
Miçangas e esferas
 Parafusos e porcas
Parafusos e porcas
 Cadinhos
Cadinhos
 Discos
Discos
 Fibras e tecidos
Fibras e tecidos
 Filmes
Filmes
 Flocos
Flocos
 Espumas
Espumas
 Folha de alumínio
Folha de alumínio
 Grânulos
Grânulos
 Favos de mel
Favos de mel
 Tinta
Tinta
 Laminado
Laminado
 Nódulos
Nódulos
 Malhas
Malhas
 Filme metalizado
Filme metalizado
 Placa
Placa
 Pós
Pós
 Vara
Vara
 Folhas
Folhas
 Cristais individuais
Cristais individuais
 Alvo de pulverização
Alvo de pulverização
 Tubos
Tubos
 Lavadora
Lavadora
 Fios
Fios
 Conversores e calculadoras
Conversores e calculadoras
 Escreva para nós
Escreva para nós




 Chin Trento
Chin Trento



